
告别“伤筋动骨一百天”?脊柱手术加速康复的22万例证据全景图
长期以来,在公众的固有认知中,脊柱手术往往与“高风险”、“剧烈疼痛”以及术后漫长的“卧床静养”画上等号。所谓“伤筋动骨一百天”,这种传统观念不仅加深了患者对手术的恐惧,也在一定程度上固化了临床护理的模式。然而,随着现代医学理念的更迭,一场名为“加速康复外科”(Enhanced Recovery After Surgery, ERAS)的静悄悄的革命正在重塑这一领域。
ERAS 理念最早起源于结直肠外科,旨在通过优化围术期的各种处理措施,减少患者的生理和心理创伤。但在脊柱外科领域(ERASS),这一理念的落地却显得有些“步调不一”。尽管越来越多的医疗机构开始尝试通过多模式镇痛、早期进食和早期下床活动来加速患者康复,但是,一个尴尬的现实横亘在医生与研究者面前:截至目前,除了针对腰椎融合术有相对明确的共识外,整个脊柱外科尚缺乏一套通用的、标准化的 ERAS 指南。这种“各自为战”的局面导致了临床证据的碎片化,让决策者难以看清全貌:在脊柱上动刀子,真的能通过这一套流程变得既快又好吗?
为了解开这一谜题,一项来自英国和意大利的联合研究团队完成了目前该领域最高级别的证据合成——“伞形评价”(Umbrella Review)。这项发表于顶刊《British Journal of Anaesthesia》的研究,将目光投向了过往的 17 项系统评价和 55 项荟萃分析,涵盖了超过 22 万名(221,605)参与者,试图为脊柱手术的加速康复绘制一张清晰的证据全景图。
1. 顶层设计的缺失与碎片的拼凑
“伞形评价”之所以重要,是因为它处于证据金字塔的塔尖——它是对“系统评价”的再评价。在医学文献浩如烟海的今天,关于脊柱 ERAS 的单一研究往往只能通过有限的样本量得出局部的结论,甚至不同研究之间会出现相互矛盾的结果(例如关于术后疼痛和再入院率的争议)。
这项研究的独特价值在于,它不仅汇总了海量数据,还通过严谨的方法学(如 AMSTAR-2 和 ROBIS 工具)剔除了低质量证据,并去除了重叠的原始研究,从而避免了数据的重复计算。研究者们将这 22 万名患者的数据重新放入统计模型中,试图回答三个核心层面的问题:宏观的医疗成本、中观的手术流程效率,以及微观的患者切身感受。
2. 核心成效:更快、更省,且并未牺牲安全性
对于医院管理者和支付方而言,效率与成本是永恒的主题;而对于患者,住院时间的长短直接关系到生活质量的恢复。研究数据给出了一份令人振奋的答卷:ERAS 协议的实施,显著提升了脊柱手术的流转效率。
2.1 住院天数与经济账
数据表明,实施 ERAS 协议后,患者的平均住院时间(LOS)显著缩短了 1.55 天。在医疗资源日益紧张的今天,这看似不起眼的 1.5 天,意味着床位周转率的大幅提升。更直观的冲击来自经济层面——每位患者的医疗成本平均降低了 1029.41 美元。这种成本的下降并非源于偷工减料,而是源于并发症的减少和住院日的缩短。
为了更直观地理解这些数据背后的统计学意义,我们需要借助“森林图”来审视这些证据的分布。如图[1]所示,这是一张涵盖了住院时间、再入院率和成本的荟萃分析图谱。
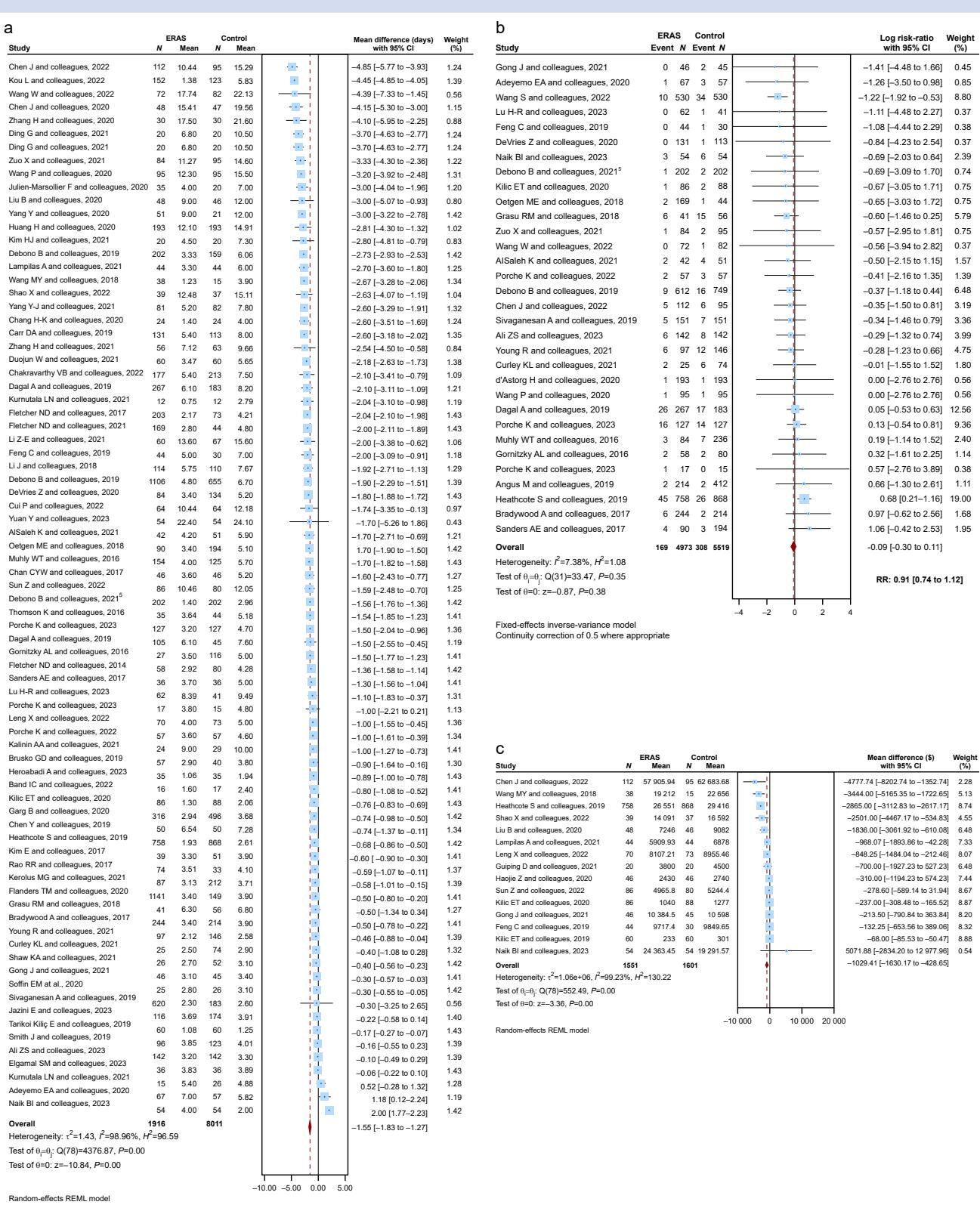
从图[1]的左侧部分(a子图)我们可以清晰地看到,绝大多数代表住院时间(Length of stay)的研究点都落在了中线的左侧,这意味着 ERAS 组的住院时间普遍短于传统对照组,汇总后的菱形图标也明确指示了显著的统计学差异。同样,在图[1]的右下角(c子图)关于成本(Cost)的分析中,数据点也呈现出类似的一边倒趋势,有力地支撑了 ERAS 能够“省钱”的结论。
2.2 再入院率:并没有因为“赶人出院”而反弹
一个常见的担忧是:让患者早早出院,会不会导致他们因为病情反复而不得不再次入院?这不仅会增加医疗负担,更是对患者安全的威胁。研究者对 32 项相关研究进行了深入分析。
当我们再次把目光投向图[1]的右上部分(b子图,Readmission rate)时,会发现情况变得微妙起来。与住院时间和成本那种一边倒的趋势不同,这里的很多研究横线跨越了中线(即无效线),且汇总后的菱形图标虽然偏向左侧(提示再入院率有 9% 的下降趋势),但其统计学上的 P 值仅为 0.38。这意味着,目前的证据表明 ERAS 既没有显著降低,也没有增加再入院率。这是一个至关重要的“非劣效性”发现——它告诉我们,缩短住院时间并没有以牺牲患者的安全为代价,患者并未因“被赶出院”而被迫“二进宫”。
3. 安全与舒适的双重奏:并发症与阿片类药物的退潮
如果说“快”和“省”是医院运营的指标,那么“安”和“舒”则是患者最在乎的体验。在这方面,ERAS 协议展现出了令人信服的保护力。
3.1 告别并发症的阴霾
手术并发症是每一位外科医生和患者的噩梦。令人欣慰的是,研究发现实施 ERAS 协议后,术后并发症的风险显著降低了 39%(相对风险 RR = 0.61)。这可能得益于早期的下床活动促进了血液循环,减少了血栓风险,以及优化的液体管理减少了组织水肿。
这一结论在图[2]的左侧部分(a子图)得到了有力的视觉印证。在这张展示术后并发症发生率的森林图中,我们可以看到密集的横线集中在中线的左侧,这意味着在纳入的 54 项原始研究中,绝大多数都支持 ERAS 能有效减少并发症。这种一致性极高的“左偏”趋势,为临床医生推广加速康复理念提供了坚实的信心。

3.2 拒绝阿片类药物依赖
在传统的脊柱手术后,为了镇压剧痛,阿片类药物(如吗啡)往往是标配。然而,这类药物带来的恶心、呕吐以及潜在的成瘾风险不容忽视。ERAS 强调“多模式镇痛”,即通过不同作用机制的非阿片类药物联合使用,来减少对单一强效镇痛药的依赖。
数据证实了这一策略的成功:在术后 24 小时内,ERAS 组患者的阿片类药物消耗量平均减少了 7.26 毫克(吗啡当量)。如图[2]右下角(c子图)所示,代表药物消耗量的森林图清晰地展示了这一显著的下降趋势,这标志着脊柱外科正在向“无阿片化”或“少阿片化”的绿色镇痛时代迈进。
3.3 疼痛评分的“尴尬”现实
有趣的是,尽管药物用量少了,但患者报告的疼痛评分(VAS/NRS)并没有出现统计学上的显著下降(仅下降 0.27 分,P=0.19)。当我们审视图[2]右上角(b子图)关于疼痛评分的分析时,会发现数据点的分布相对离散,且置信区间跨越了中线。这或许揭示了一个临床真相:ERAS 的目标可能不是彻底消除疼痛(这在大型脊柱手术中极难实现),而是在将疼痛控制在可接受范围内的同时,最大程度地减少药物副作用并恢复身体机能。
4. 被遗忘的拼图:我们离完美的 ERAS 还有多远?
尽管上述成果令人鼓舞,但这项伞形评价也无情地揭示了当前研究的短板。ERAS 是一个包含术前、术中、术后数十项措施的庞大系统,但在实际执行和研究中,很多元素被“选择性忽略”了。
研究者利用一张热力图(Heatmap)形象地展示了这一现状。如图[3]所示,这张图谱的纵轴列出了 ERAS 协议的各个阶段,横轴则代表了纳入分析的各项研究。图中深红色的方块代表该元素在研究中未被实施或提及,而蓝色则代表已包含。
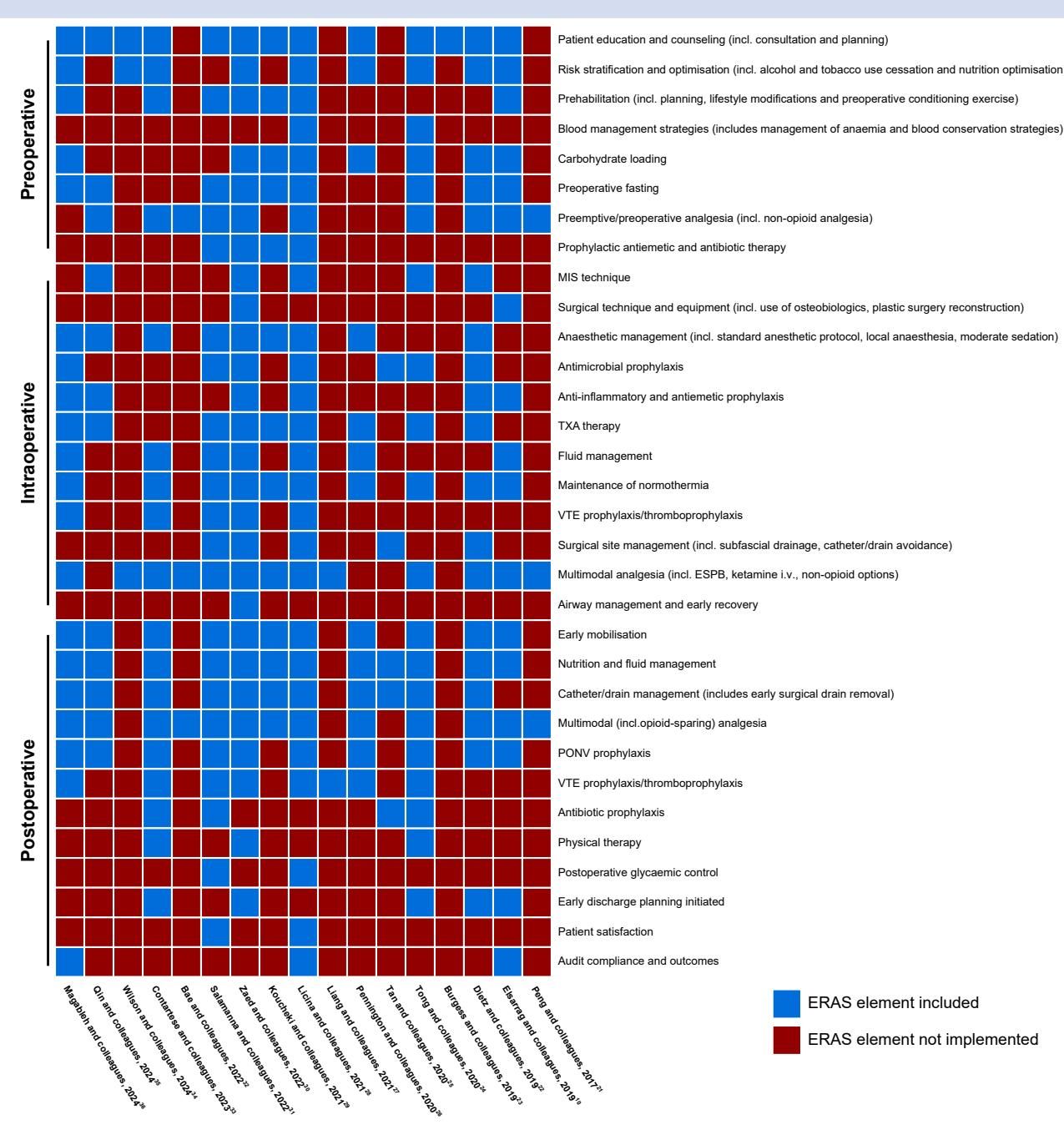
从图[3]中我们可以一眼看出这种“冷热不均”:
- 热门区域:术前“患者教育与咨询”以及术后“多模式镇痛”几乎全是蓝色,说明这些是目前公认且执行度高的核心措施。
- 冷门死角:反观其他区域,如术前的“血液管理策略”、“预防性止吐”,以及术后的“血糖控制”、“物理治疗”和“审计依从性”,则大片呈现红色。
这张图告诉我们,目前的“加速康复”往往是“缺胳膊少腿”的。我们在健康宣教和止痛上做得很好,但在精细化的代谢管理、血液保护以及对医疗行为本身的质量监控(审计)方面,仍有巨大的提升空间。这些未被充分探索的“红色区域”,或许正是未来进一步提升脊柱手术疗效的潜在金矿。
5. 结语:通往标准化的未来
综上所述,这项涉及 22 万人的宏大回顾为脊柱外科的未来指明了方向:加速康复(ERAS)不仅是可行的,而且是必须的。它在不增加再入院风险的前提下,实实在在地缩短了住院时间、降低了医疗成本、减少了并发症,并让患者少吃了不少阿片类药物。
然而,我们也必须清醒地看到,当前的证据大多来自异质性较高的观察性研究,且对 ERAS 元素的执行存在明显的碎片化。未来的脊柱外科需要从“各自为战”的经验医学,走向基于标准化指南的精准医疗。我们需要更多高质量的随机对照试验(RCT),去填补那些热力图上的“红色死角”,去探索针对不同术式(如微创 vs 开放,颈椎 vs 腰椎)的特异性 ERAS 方案。
对于患者而言,这意味着告别“伤筋动骨一百天”的旧历,迎接一个更安全、更舒适、更快速复原的新时代。
论文信息
- 标题:Optimising postoperative spine outcomes: an umbrella review of enhanced recovery after spinal surgery (ERASS) protocols.
- 论文链接:https://doi.org/10.1016/j.bja.2025.08.037
- 发表时间:2025-12
- 期刊/会议:British journal of anaesthesia
- 作者:Daniel Sescu, Devika Dahiya, Laura Scaramuzzo, ..., Andreas K Demetriades
本文由超能文献AI辅助创作,内容仅供学术交流参考,不代表任何医学建议。
References
- https://wilddata-cms-1320403996.cos.ap-shanghai.myqcloud.com/news/articles/20251203/oyqay5s5jfgj6rihq0jws067_1_a16930fa0a.jpg
- https://wilddata-cms-1320403996.cos.ap-shanghai.myqcloud.com/news/articles/20251203/oyqay5s5jfgj6rihq0jws067_2_3275215df8.jpg
- https://wilddata-cms-1320403996.cos.ap-shanghai.myqcloud.com/news/articles/20251203/oyqay5s5jfgj6rihq0jws067_3_8b95ec470f.jpg
分享
推荐阅读

合成舌头检测辣椒辣度:牛奶蛋白启发的传感器革新食品安全检测
华东理工大学团队研发出受牛奶启发的酪蛋白凝胶传感器,可精确测量辣椒辣度,避免人工品尝风险。这项发表于ACS Sensors的技术有望革新食品质量控制标准。

哈佛AI模型识别123个新罕见病基因:诊断从十年缩至数小时
哈佛医学院popEVE模型利用进化数据预测致病变异,将罕见病诊断时间从平均5.6年大幅缩短。30000例疑难病例中三分之一获得诊断,123个新疾病基因被发现。

诺奖得主实验室新突破:AI从零设计出原子级精准抗体
2024年11月5日,就在David Baker因蛋白质设计获得诺贝尔化学奖不到一个月后,他的实验室在《Nature》发表了一项更激进的成果:用AI从零开始设计抗体,精度达到单个原子的尺度。这是生物医药产业的分水岭时刻。

化疗神经损伤的"幕后黑手"找到了:不是神经细胞,而是免疫细胞在作祟
威尔康奈尔医学院和维克森林大学最新研究揭示,化疗药物紫杉醇通过激活免疫细胞中的IRE1α应激通路引发神经损伤,而非直接损伤神经。这一发现为困扰半数化疗患者的周围神经病变提供了全新治疗思路,相关抑制剂已进入临床试验。

MIT开源BoltzGen:AI设计蛋白质药物,向"不可成药"靶点宣战
MIT团队推出开源AI模型BoltzGen,在26个挑战性靶点上实现纳摩尔级结合亲和力,67%成功率打破蛋白质设计困境,免费商用或颠覆制药行业格局。

超加工食品的全球警报:《柳叶刀》揭示人类健康的隐形杀手
覆盖104项研究的综合分析显示,92%的研究证实超加工食品与慢性病相关。这场由跨国食品公司主导的饮食革命,正在成为21世纪最严重的公共卫生威胁之一。