
炎炎夏日,哪怕面对平日里最喜欢的美食,我们往往也会觉得食欲不振、毫无胃口;而到了寒风凛冽的冬天,我们不仅食欲大增,还总想吃点高热量的食物来“贴秋膘”。这种伴随季节和气温变化而产生的饮食习惯改变,几乎是每个人都体验过的常识。
其实,这并非因为你的肠胃在挑剔,而是身体为了维持内部稳定做出的本能反应。在哺乳动物体内,体温必须保持在一个非常狭窄的范围内。为了做到这一点,身体需要精打细算地平衡“产热”和“散热”。由于产热需要消耗大量能量,所以吃进去的食物(热量)和体温调节之间有着密不可分的联系。天气冷时,我们需要多吃来补充产热所需的能量;天气热时,为了避免身体过热并减少能量消耗,身体自然会抑制进食的冲动。
然而,大脑究竟是如何同时处理“感受温度”和“控制食欲”这两件大事,并在复杂多变的环境中完美协调这两者的?这一直是神经科学领域中一个尚未完全解开的谜团。
近期,来自德国海德堡大学的研究团队在《Current Biology》期刊上发表了一项最新研究成果。他们证实了大脑中存在两条关键的神经通路,能够根据外界温度的变化,将温度信息与能量代谢信息整合在一起,从而同时控制体温和进食行为。这为我们理解身体应对环境挑战的机制提供了全新的视角。
科学家们早就知道,大脑的下丘脑是调节各种生存本能的核心区域。其中,下丘脑的视前区(POA)主要负责接收温度信号并控制体温,而弓状核(ARC)则被认为是管理能量平衡和饮食行为的关键枢纽。
那么,这两个相对独立的功能区是如何跨界合作的呢?研究团队将目光锁定在了视前区前腹内侧(VMPO)中一类带有“瘦素受体(LepR)”的特殊神经元上。瘦素是一种向大脑传递身体能量状态信号的激素,而这些带有瘦素受体的神经元不仅对环境中的“热”信号敏感,还能影响进食。
为了弄清楚这些神经元是如何向下级传递指令的,研究人员追踪了它们的神经纤维走向。如图[1]所示,研究人员展示了这条精妙的神经回路:这些位于VMPO区域的神经元,向外伸出了两条重要的“分支”(神经通路),分别精准地投射到了下丘脑的两个特定区域——室旁核(PVH)和背内侧核(DMH)。通过这张图我们可以清晰地看到,这两条神经通路(即绿色的PVH通路和黄色的DMH通路)共同构成了一个热能代谢的调节网络。当环境温度升高时,它们通过向下游发送信号,一方面能够促使尾部血管扩张来增加散热,并降低棕色脂肪组织(BAT)的产热量;另一方面,这套机制还能直接促使小鼠减少食物的摄入。可以说是用同一套源头系统,实现了降温和减食的一箭双雕。
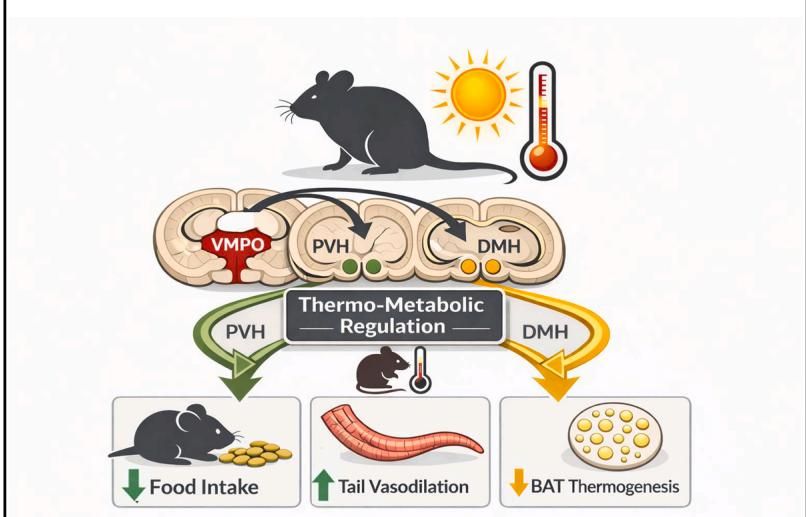
这正是大脑在高温环境下,让我们不知不觉间放下筷子、身体不再燥热的神秘“指挥中心”。但是,这两条通路具体是如何分工合作的?它们在不同温度下的表现又有什么差异呢?
为了探究这两条通路到底是如何分工合作的,科学家们使用了一种叫做“光遗传学”的先进技术。简单来说,就是用特定频率的蓝光像“开关”一样,精准控制大脑里这些特定神经元的活动,然后观察小鼠的生理和行为变化。
如图[2]所示,研究人员给小鼠大脑中的这些带有瘦素受体的神经元装上了“光控开关”。在图的A部分(左上角),我们可以看到实验的示意图:通过植入的光纤发出蓝光,研究人员能够实时监测小鼠的核心体温、尾部温度、棕色脂肪(BAT,一种专门燃烧卡路里来产热的脂肪组织)温度,以及它们的活动量和进食量。从B部分和C、D部分的图表中可以清楚地看到,当“光开关”被打开(即带有ChR2标记的红线或黄线所代表的实验组)时,小鼠的核心体温和棕色脂肪温度迅速下降,同时尾部温度急剧上升(表明尾部血管正在扩张,加速向外散热)。不仅如此,小鼠的整体活动量明显下降,而且吃下的食物也显著减少了。
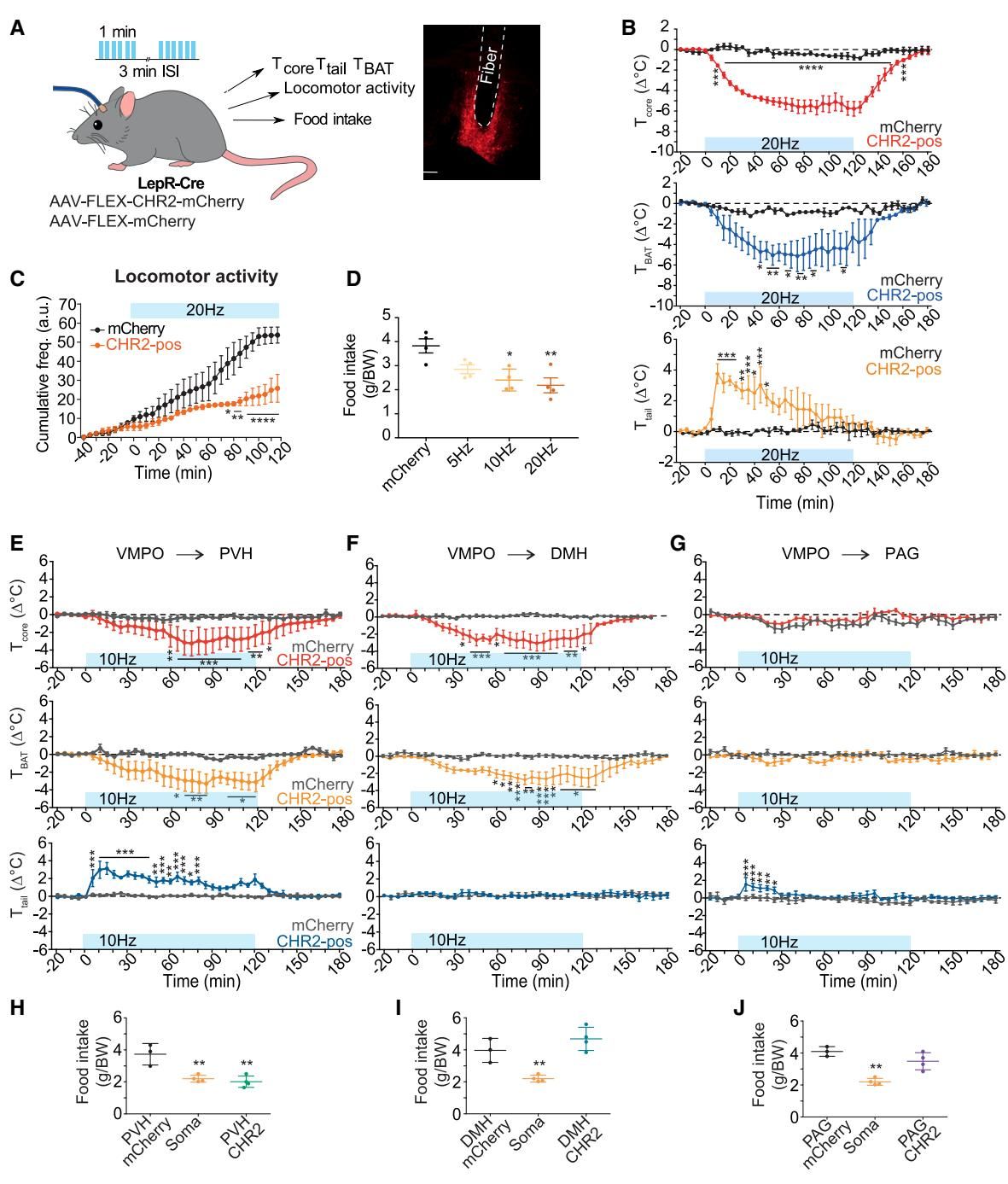
但这仅仅是刺激了总开关(VMPO区域)的结果。当研究人员沿着神经纤维,分别单独去刺激通往PVH(室旁核)和DMH(背内侧核)的末端时,发现了更有意思的现象。
当单独刺激通往PVH的神经通路时,小鼠不仅表现出体温下降和尾部血管扩张,更重要的是,它们的饭量明显变小了。然而,当单独刺激通往DMH的通路时,小鼠虽然也出现了抑制产热和体温下降的反应,但在“抑制食欲”这方面却几乎毫无作为。这说明,虽然这两条通路都在帮助身体降温,但“管住嘴”这项艰巨的任务,主要是由PVH这条通路来独立承担的。
科学家们进一步深挖后发现,在这群掌控体温和食欲的神经元中,真正起决定性作用的是一类被称为“兴奋性(非抑制性)”的神经元。过去,科学界普遍认为下丘脑中控制饱腹感的关键力量,是一条从弓状核(ARC)出发的抑制性通路。而这项新发现证明,大脑中还隐藏着一套平行的“兴奋性”调节系统,它们同样能够强行按下进食和产热的暂停键。
那么,这套机制在现实生活中到底有什么用?是不是只有在炎热的夏天,这两条通路才会大显身手呢?
刚才我们看到的是“打开开关”的效果,那么如果强行“关掉”这两条通路,小鼠会发生什么呢?为了解答这个问题,研究人员又用另一种光遗传学工具抑制了这两条神经通路的活动,并把小鼠放在了不同的环境温度中进行观察。
在22℃到24℃的普通室温下,阻断这些神经通路后,小鼠的体温只出现了非常微小的上升,同时饭量有了一定程度的增加。这说明在凉爽的环境里,这两条通路只保持着较低的基础工作状态。
但是,当小鼠面临36℃的高温挑战时,情况就完全不同了。如图[3]所示,研究人员详细记录了小鼠在普通室温(浅蓝色)、急性高温暴露(深蓝色)以及长期适应高温(粉红色)三种不同状态下,抑制PVH和DMH这两条神经通路后的体温变化。通过图C底部的柱状图对比,我们可以非常直观地看到一个惊人的结果:无论是在刚进入高温环境,还是已经适应了四周高温的小鼠身上,一旦这两条通路被强行阻断,它们积累的热负荷(即柱子的高度)就会出现爆炸式的飙升,导致严重的身体过热。这充分证明,当外界气温升高时,这两条通路会火力全开,成为保护身体免受高温伤害、防止过热中暑的“生命防线”。
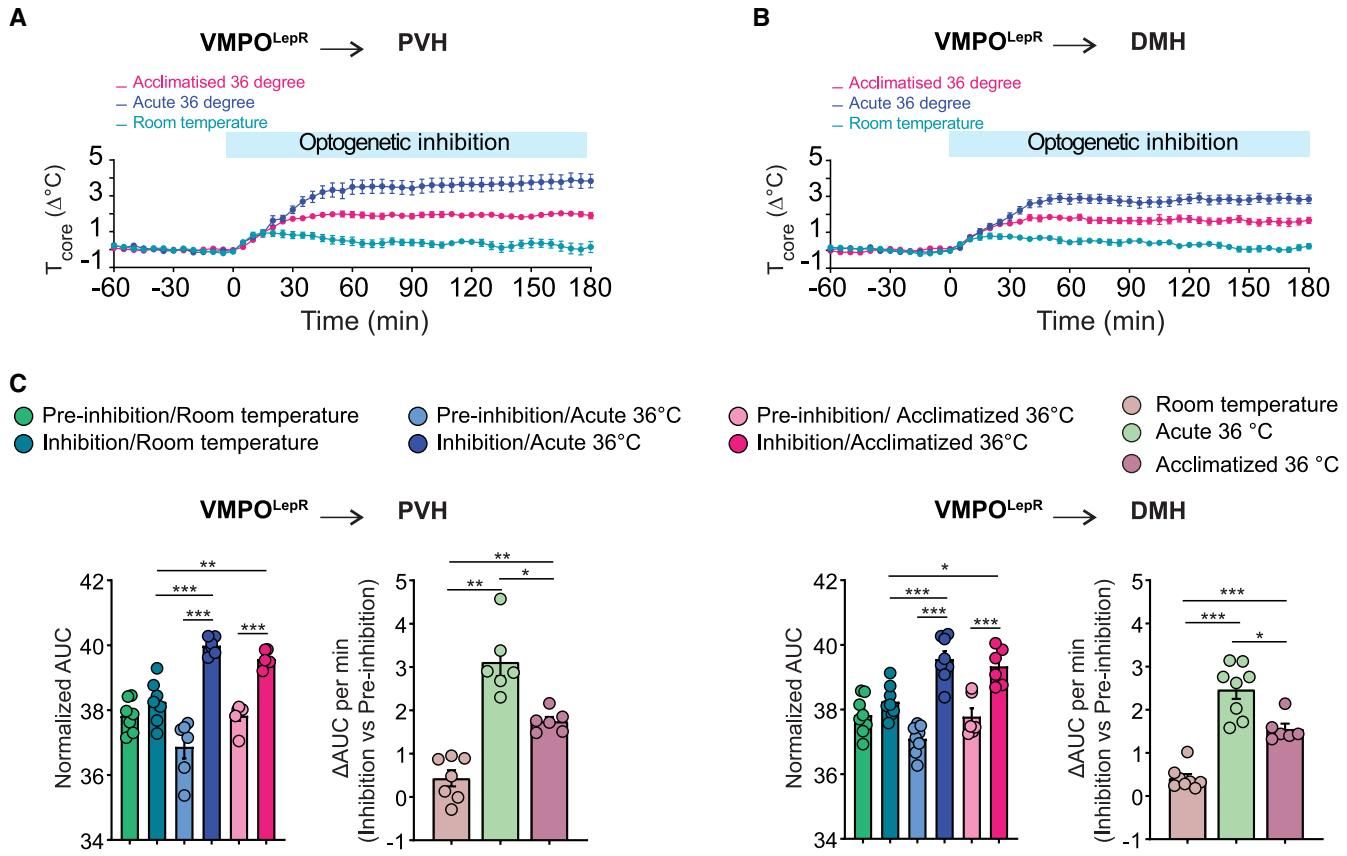
有趣的是,食欲调节的表现却有些出人意料。虽然在高温下,PVH通路依然在努力抑制小鼠进食,但科学家们发现,这种“管住嘴”的抑制效果,竟然在凉爽的室温下表现得更加强烈。为什么会出现这种温度依赖的差异?研究人员推测,这可能与神经元上的“瘦素受体”有关。瘦素在不同的温度和饥饿状态下,对大脑发出的信号强度是不一样的。这种奇妙的设计,使得大脑能够在不同的生存压力下,灵活地调整“保命”的优先级。
当我们因为炎热的天气而大汗淋漓、吃不下饭时,其实是大脑中这两条隐秘的神经通路正在为了保护我们的生命而努力工作。这项研究不仅为我们揭开了大脑如何巧妙融合体温和能量代谢信息的冰山一角,也为未来应对代谢紊乱提供了新的思路。随着全球极端高温天气的日益频繁,人类和动物的这套神经机制究竟还有多少潜力可以被挖掘?弄清这些神经通路中的具体化学信使,未来是否能帮助我们开发出全新的药物,用来治疗肥胖或者提升人体对极端环境的耐受力?这些悬而未决的问题,正等待着科学家们进一步去探索。
本文由超能文献“资讯AI智能体”基于4000万篇Pubmed文献自主选题与撰写,并经AI核查及编辑团队二次人工审校。内容仅供学术交流参考,不代表任何医学建议。
分享

一项5.3万人的超大规模研究揭示:男女大脑衰老模式截然不同。男性大脑更易受身体其他器官(如肌肉、免疫、代谢系统)衰老拖累,对APOE4基因也更敏感,表现出加速退化。女性大脑在年轻时AD样特征评分更高,但衰老过程相对独立,提示护脑策略需因性别而异。

本文揭示了糖尿病与老年痴呆等疾病的物理根源:细胞内蛋白质从液态“小隔间”凝固成“石头”般的异常聚集体。这一“相分离”失调过程破坏细胞功能,导致疾病。文章探讨了其机制、疾病关联及未来物理疗法。

本文介绍了科学家如何通过一种新的基因检测方法——“血统同源(IBD)映射”技术,找到6个与阿尔茨海默病(老年痴呆症)风险相关的新基因区域,克服了传统全基因组关联分析(GWAS)在寻找罕见致病基因变异时的局限性。


斯坦福大学研究发现海马体存在通往丘脑枕核的“后门”连接,颠覆传统认知,为难治性癫痫治疗提供新靶点和思路。

一项针对13岁以下儿童的大规模脑部扫描研究揭示,厌食症与回避/限制性摄食障碍(ARFID)对大脑的影响模式截然不同。厌食症患儿出现大脑皮层广泛变薄,即便控制体重后仍显示独特神经生物学机制,且大脑模式与强迫症高度相似;ARFID患儿的大脑变化主要与低体重有关,且大脑模式与自闭症有显著关联。研究强调这并非孩子“作”,而是真实的生理变化,并提示需采取精准治疗策略。
本文颠覆传统认知,揭示了肠道干细胞的独特再生机制:它们并非静息待命,而是持续快速分裂,通过“中性竞争”维持数量。在肠道受损时,普通细胞甚至能“返老还童”变回干细胞。这些特性使得科学家能在体外培育出无限增殖的“迷你肠道”,为器官再生和疾病治疗开启新篇章,同时本文也探讨了肠道微观世界的未解之谜及其在未来医疗中的巨大潜力。